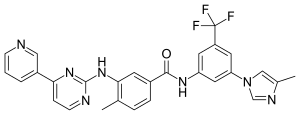
尼洛替尼
 | |
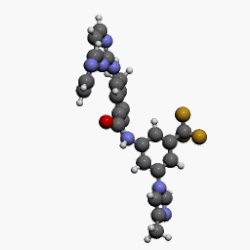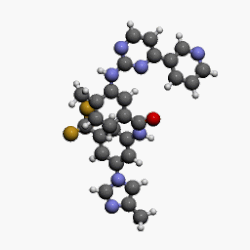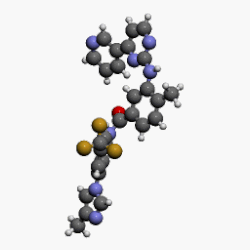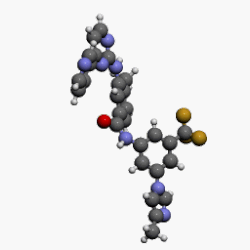 | |
| 临床资料 | |
|---|---|
| 核准状况 | |
| 给药途径 | Oral |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 生物利用度 | 30% |
| 血浆蛋白结合率 | 98% |
| 药物代谢 | 胆 |
| 生物半衰期 | 17 h |
| 排泄途径 | 胆道 |
| 识别信息 | |
| |
| CAS号 | 641571-10-0((base)) |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.166.395 |
| 化学信息 | |
| 化学式 | C28H22F3N7O |
| 摩尔质量 | 529.5245 g/mol |
| 3D模型(JSmol) | |
| |
| |

尼洛替尼(英语:Nilotinib),是由瑞士诺华公司研制销售[1],治疗慢性骨髓性白血病的第二代/新一代标靶药物[2]。在一项I型临床试验中,尼洛替尼被发现,其也因其临床编号称之为AMN107。该药药效安全,并对治疗慢性骨髓性白血病/慢性粒细胞性白血病患者服用伊马替尼(英语:imatinib)而产生的抗药性有很好的疗效。[3]在一项研究调查中,92%的患者(已经出现抗药性或药效迟钝性)通过五个月的疗程而获得了正常的白细胞总量标准[4]。是一种酪氨酸激酶抑制剂,其含量主要抑制BCR-ABL[5]、KIT、LCK、EPHA3、EPHA8、DDR1、DDR2、PDGFRB、MAPK11、ZAK激酶等。2007年,该药已被美国FDA批准用于治疗慢性骨髓性白血病。及后于2009年, 被欧盟EMA批准治疗慢性骨髓性白血病。于2011年,于香港得到批准发售[2]。2022年10月,诺华与药品专利池达成协议,授权生产尼洛替尼的仿制药供应予中低收入国家使用[6]。
使用[编辑]
此药已在美国和欧盟注册为达希纳(英语:Tasigna),其主要用于针对治疗慢性骨髓性白血病/慢性粒细胞性白血病的一线口服标靶治疗药物。
此药物分为150毫克及200毫克。
需每天服药两次,每次服药须相隔12小时。 例如第一剂药于早上十时服用,第二剂药应在晚上十时服用。
需留意,用膳前两小时之内及用膳后一小时内皆不宜服药。接受尼洛替尼治疗疗程间,切勿进食西柚或饮用西柚汁。
医疗用途[编辑]
尼洛替尼是用于治疗慢性骨髓性白血病/慢性髓细胞性白血病(CML)的一线口服标靶治疗药物。
治疗[编辑]
治疗方案的演进: 1990年代或以前,使用化疗干扰素及骨髓移植;21世纪,加入标靶治疗药物(酪氨酸激酶抑制剂 Tyrosine-Kinase Inhibitor, TKI);
最新《2013 欧洲白血病网络(ELN)治疗指引》指出[7]:
- 治疗方案3个月, BCR-ABL 病变基因数量 ≤10% (MR1)
- 治疗方案6个月, BCR-ABL 病变基因数量 <1% (MR2)
- 治疗方案12个月, BCR-ABL 病变基因数量 ≤0.1% (MR3)
- BCR-ABL 病变基因数量 ≤0.0032% (即MR 4.5)为深层分子反应,基因达无法检测(undetectable)
临床数据显示,达MR4.5的患者,可使病情不会再恶化。
临床实验结果[编辑]
ENESTnd研究指出新一代尼洛替尼与旧一代伊马替尼相比[8]:
- 于三个月时达致BCR/ABL病变基因的≤10% ,接受尼洛替尼的病人有91%达标, 而接受伊马替尼的病人有67%达标
- 于12个月时达致BCR/ABL病变基因的≤0.1% , 接受尼洛替尼的病人有44%达标, 而接受伊马替尼的病人有22%达标
- 于60个月时达致BCR/ABL病变基因的≤0.0032% (即MR 4.5水平)的百分比 , 接受尼洛替尼的病人有54%达标, 而接受伊马替尼的病人有31%达标
研究指出, 新一代尼洛替尼与旧一代伊马替尼相比, 有更佳的医疗效果。
其他有关尼洛替尼一线治疗的研究有ENEST1st,其显示尼洛替尼能令病人迅速达成深度反应,12个月时累计21%病人获得MR4.5,24个月时更达到39%,几乎翻倍[9]。更多研究有关二线尼洛替尼的有效性和安全性。ENESTcmr比较伊马替尼服用2年后转用尼洛替尼和继续伊马替尼的效果,结果显示尼洛替尼达到MR4.5的中位时间是24个月,而伊马替尼甚至在48个月时也未达到[10]。2101研究显示,二线转用尼洛替尼可令病人达到最佳治疗反应[11];4年总体估计生存率达78%[12]。ENRICH研究显示因低级数慢性不良事件而由伊马替尼转用尼洛替尼的病人,其中一半获得了MR4.5,并且生活质素获得了整体改善[13]。
TKI 治疗获得深度分子学反应持续超过2年的CML患者部分能够获得长期的无治疗缓解(treatment free remission, TFR),即功能性治愈。最新的ENESTfreedom研究证实了这个观点[14]。
- 尼洛替尼停药96周后,48.9% (93/190)的病人仍处于TFR阶段并维持MMR,还有88个病人维持MR4.5
- 46.3%(88/190)病人由于失去MMR而重启尼洛替尼治疗,经过中位数为7周的治疗后,98.9%(87/88)的病人重新获得MMR
- 与肌肉骨骼痛相关的不良事件的频度于TFR的首48周内,与巩固期比较(17%)出现上升(34%),随后在第二个48周内出现下降(9.0%)
- ENESTop研究则显示,163名伊马替尼治疗失败后接受二线尼洛替尼治疗的病人,77.3% (126/163)达到了TFR的标准,58%与53%的病人分别在48周与96周时仍维持 TFR[15]。
参考文献[编辑]
- ^ 重磅 诺华3个产品及新适应症纳入国家医保谈判药品目录,6个目录内产品原有适应症成功续约. 诺华中国. [2023-01-12].
- ^ 2.0 2.1 口服標靶藥物病人須知尼洛替尼Nilotinib. 医院管理局. [2023-01-12]. (原始内容存档于2023-01-12).
- ^ Kantarjian H; et al. Nilotinib in imatinib-resistant CML and Philadelphia chromosome-positive ALL. N Engl J Med. 2006, 354 (24): 2542–51. PMID 16775235. doi:10.1056/NEJMoa055104.
- ^ Patients with treatment-resistant leukemia achieve high responses to Tasigna (nilotinib) in first published clinical trial results. MediaReleases (Novartis). 2006-06-14 [2009-08-04]. (原始内容存档于2011-07-09).
- ^ Weisberg E, Manley P, Mestan J, Cowan-Jacob S, Ray A, Griffin JD. AMN107 (nilotinib): a novel and selective inhibitor of BCR-ABL. Br. J. Cancer. June 2006, 94 (12): 1765–9. PMC 2361347
 . PMID 16721371. doi:10.1038/sj.bjc.6603170.
. PMID 16721371. doi:10.1038/sj.bjc.6603170.
- ^ Novartis seals deal to license high-priced cancer drug. swissinfo.ch. 2022-10-22 [2023-01-12]. (原始内容存档于2023-01-25).
- ^ Baccarani M, Deininger MW, Rosti G, et al. European LeukemiaNet recommendations for the management of chronic myeloid leukemia: 2013. Blood. 2013; 122(6): 872-84.
- ^ Hochhaus A, Saglio G, Hughes TP, et al. Long-term benefits and risks of frontline nilotinib vs imatinib for chronic myeloid leukemia in chronic phase: 5-year update of the randomized ENESTnd trial. Leukemia. 2016; 30(5): 1044–1054.
- ^ Hochhaus A, et al.Frontline nilotinib in patients with chronic myeloid leukemia in chronic phase: results from the European ENEST1st study. Leukemia. 2016; 30(1): 57-64.
- ^ Hughes TP, et al. Sustained deep molecular responses in patients switched to nilotinib due to persistent BCR-ABL1 on imatinib: final ENESTcmr randomized trial results. Leukemia. 2017; 31: 2529–31.
- ^ Kantarjian HM, et al. Nilotinib is effective in patients with chronic myeloid leukaemia in chronic phase after imatinib resistance or intolerance: 24-month follow-up results. Blood. 2011;117:1141-45.
- ^ Giles FJ, et al. Nilotinib in imatinib-resistant or imatinib-intolerant patients with chronic myeloid leukemia in chronic phase: 48-month follow-up results of a phase II study. Leukemia. 2013;27(1):107-112.
- ^ Cortes J, et al. Clin Lymphoma Myeloma Leuk. Evaluating the impact of a switch to nilotinib on imatinib-related chronic low-grade adverse events in patients with CML-CP: the ENRICH study. 2016; 16(5): 286-296.
- ^ Ross DM, et al. Durable treatment-free remission in patients with chronic myeloid leukemia in chronic phase following frontline nilotinib: 96-week update of the ENESTfreedom study. J Cancer Res Clin Oncol. 2018 Feb 22. [Epub ahead of print].
- ^ Mahon FX, et al.Treatment-Free Remission After Second-Line Nilotinib Treatment in Patients With Chronic Myeloid Leukemia in Chronic Phase: Results From a Single-Group, Phase 2, Open-Label Study. Ann Intern Med. 2018 Feb 20. [Epub ahead of print]
参见[编辑]
- Bcr-Abl酪氨酸激酶抑制剂(Bcr-Abl tyrosine-kinase inhibitor、Bcr-Abl TKI))
- 酪氨酸激酶抑制剂
- ABL激酶结构域(ABL (gene))
外部链接[编辑]
- New drug information/Abbreviated Scientific Narrative
- Highlights of Prescription information Nilotinib (August 2007) Novartis Pharmaceuticals Corporation (USA)
- Summary of Product Characteristics Nilotinib (November 2007) Novartis AG (Europe)
| ||||||||||||||||||||||||||||||||||||||||||||||||
