十羰基二铼
| 十羰基二铼 | |
|---|---|

| |
| |

| |
| IUPAC名 bis(pentacarbonylrhenium)(Re—Re) | |
| 别名 | 羰基铼、五羰基铼 |
| 识别 | |
| CAS号 | 14285-68-8 |
| PubChem | 518917 |
| ChemSpider | 436546 |
| SMILES |
|
| InChI |
|
| InChIKey | ZIZHEHXAMPQGEK-UHFFFAOYAX |
| 性质 | |
| 化学式 | Re2(CO)10 |
| 摩尔质量 | 652.52 g/mol g·mol⁻¹ |
| 熔点 | 170 °C(443 K) |
| 溶解性(水) | |
| 危险性 | |
| 警示术语 | R:R20 |
| 安全术语 | S:S36 |
| 欧盟分类 | 有害(Xn)
|
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
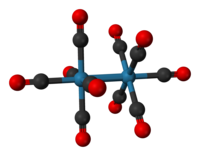
十羰基二铼是一种无机化合物,分子式为Re2(CO)10。它可以购得,经常用作合成各种铼羰基配合物的起点。它首次于1941年由瓦尔特·希贝尔记录,他通过将铼还原羰基化制备这个化合物。[1]十羰基二铼中有一对由一个Re-Re键连接的四角锥形Re(CO)5单元,形成一个全同羰基配合物。[2]
结构及性质[编辑]
十羰基二铼的晶体结构相当熟知。化合物由一对四角锥形的Re(CO)5单位组成,而它们由一个Re-Re键连接。此处可以发生两种构象:交错式和重叠式。重叠式构象占所有构象的30%,它会产生一个D4h点群,但点群为D4d的交错式比较稳定。Re-Re键长通过实验发现为3.04Å。[3]
合成[编辑]
十羰基二铼可以由七氧化二铼(Re2O7)在350 atm和250 °C下还原羰基化制备。
- Re2O7 + 17 CO → Re2(CO)10 + 7 CO2
反应[编辑]
羰基配体可以被其他如膦和亚磷酸盐的配体(以L标记)置换。[4]
- Re2(CO)10 + 2 L → Re2(CO)8L2
这个化合物也可以通过卤化“破裂”成单核Re(I)羰基配合物:[5]
- Re2(CO)10 + X2 → 2 Re(CO)5X (X = Cl, Br, I)
加入溴就会生成五羰基溴化铼。它是许多铼配合物的中间体。这个化合物也可以氢化生成各种多铼配合物,最终得到铼元素。[6]
- Re2(CO)10 → H3Re3(CO)12 → H5Re4(CO)12 → Re (metal)
十羰基二铼遇水时,就会经过光解作用转化为羟基配合物:[7]
- Re2(CO)10 → HRe(CO)5 + Re4(CO)12(OH)4
应用[编辑]
铼基催化作用可用于复分解反应、重整、氢化以及各种如加氢脱硫的加氢处理过程。[8]十羰基二铼可以用来促进醇的硅烷化(silylation)并制备硅醚,其反应为:[9]
- RSiH3 + R'OH → RH2SiOR' + H2
参见[编辑]
参考文献[编辑]
- ^ W. Hieber; H. Fuchs. Über Metallcarbonyle. XXXVIII. Über Rheniumpentacarbonyl. Zeitschrift für anorganische und allgemeine Chemie. 1941, 248 (3): 256–268. doi:10.1002/zaac.19412480304 (德语).
- ^ F. Armstrong; J. Rourke; M. Hagerman; M. Weller; P. Atkins; T. Overton. Shiver and Atkins' Inorganic Chemistry 5th edition: 555. 2010.
- ^ M. Churchill; K. Amoh; H. Wasserman. Redetermination of the crystal structure of dimanganese decacarbonyl and determination of the crystal structure of dirhenium decacarbonyl. Revised values for the manganese-manganese and rhenium-rhenium bond lengths in dimanganese decacarbonyl and dirhenium decacarbonyl. Inorganic Chemistry. 1981, 20 (3): 1609–1612. doi:10.1021/ic50219a056.
- ^ K.S. Suslick; P.F. Schubert. Sonochemistry of dimanganese decacarbonyl (Mn2(CO)10) and dirhenium decacarbonyl (Re2(CO)10). Journal of the American Chemical Society. 1983, 105 (19): 6042–6044. doi:10.1021/ja00357a014.
- ^ Steven P. Schmidt; William C. Trogler; Fred Basolo. Pentacarbonylrhenium Halides. Inorganic Syntheses 28. 2007: 154–159. ISBN 9780470132593. doi:10.1002/9780470132593.ch42.
- ^ C. Dossi, J. Schaefer, W. M. H. Sachtler. Mechanism of particle formation in decomposing Re2(CO)10 on NaY and NaHY zeolites: effect of prereduced Pt clusters in the supercages. Journal of Molecular Catalysis. 1989, 52 (1): 193–209. doi:10.1016/0304-5102(89)80089-6.
- ^ D. R. Gard; T. L. Brown. Photochemical reactions of dirhenium decacarbonyl with water. Journal of the American Chemical Society. 1982, 104 (23): 6340–6347. doi:10.1021/ja00387a031.
- ^ R. Jarkko; A.P. Tapani. Controlled gas-phase preparation and HDS activity of Re2(CO)10 alumina catalysts. Catalysis Letters. 2000, 65 (4): 175–180. S2CID 96952765. doi:10.1023/A:1019006413873.
- ^ D.H.R.Barton, M.J. Kelly. Mechanism and utility of the dirhenium decacarbonyl catalyzed formation of silyl ethers. Tetrahedron Letters. 1992, 33 (35): 5041–5044. doi:10.1002/chin.199302225.
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
